

Ứng dụng AI cho ung thư tuyến giáp là gì
Ứng dụng AI cho ung thư tuyến giáp là sử dụng các thuật toán trí tuệ nhân tạo AI hỗ trợ bác sỹ phát hiện, chẩn đoán, điều trị và quản lý bệnh ung thư tuyến giáp.
Ứng dụng AI cho ung thư tuyến giáp không chỉ đơn thuần là các phần mềm tự động hóa mà là các thực thể thông minh có khả năng trích xuất các đặc trưng hình ảnh và dữ liệu phi cấu trúc mà mắt người hoặc các phương pháp thống kê truyền thống thường bỏ sót.
Về mặt chức năng, các ứng dụng này được phân loại thành ba nhóm chính:
- Chẩn đoán hỗ trợ máy tính giúp phát hiện tổn thương (CADe).
- Chẩn đoán hỗ trợ máy tính giúp phân loại bản chất tổn thương (CADx).
- Hệ thống hỗ trợ quyết định lâm sàng (CDSS) tích hợp đa phương thức.
Hệ sinh thái AI trong ung thư tuyến giáp hiện nay vận hành dựa trên bốn trụ cột dữ liệu chính
- Hình ảnh học (chủ yếu là siêu âm, CT và MRI).
- Bệnh lý học (tế bào học FNA và giải phẫu bệnh).
- Dữ liệu phân tử (genomics, transcriptomics).
- Hồ sơ lâm sàng không cấu trúc thông qua các mô hình ngôn ngữ lớn (LLMs).
Sự hội tụ của các dòng dữ liệu này giúp tạo ra một cái nhìn 360 độ tổng quan về tình trạng của bệnh nhân, từ đó cá thể hóa lộ trình điều trị một cách tối ưu.

Phạm vi ứng dụng
Dự đoán di căn hạch bạch huyết và xâm lấn
Một trong những khó khăn lâm sàng quan trọng nhất trong phẫu thuật ung thư tuyến giáp là đánh giá chính xác trước mổ tình trạng di căn hạch bạch huyết cổ (CLNM – Cervical Lymph Node Metastasis).
Điều này đặc biệt cần thiết ở nhóm bệnh nhân có kết quả hình ảnh học không phát hiện hạch bất thường, hay còn gọi là phân loại cN0.
Kết quả đánh giá này mang tính quyết định rất cao vì nó ảnh hưởng trực tiếp đến việc bệnh nhân sẽ được nạo hạch dự phòng hay chỉ cần phẫu thuật bảo tồn.
Di căn hạch bạch huyết không phải là hiện tượng hiếm gặp trong ung thư tuyến giáp.
Tỷ lệ ước tính dao động từ 30–80% các trường hợp, một khoảng biến thiên rất rộng.
Chính điều này đã cho thấy rõ mức độ khó khăn của dự đoán chính xác trước phẫu thuật.
Vấn đề cốt lõi nằm ở những hạn chế vốn có của siêu âm thông thường, phương pháp chẩn đoán hình ảnh chủ đạo được sử dụng để đánh giá các nhóm hạch bạch huyết vùng cổ.
Siêu âm truyền thống có độ nhạy đặc biệt thấp để phát hiện hạch di căn ở khoang trung tâm, với tỷ lệ phát hiện chỉ đạt khoảng 20–41%.
“Vùng mù” chẩn đoán tạo ra một tình thế tiến thoái lưỡng nan đầy nan giải với hai kịch bản đều không mong muốn.
Một mặt, các hạch di căn ẩn có thể bị bỏ sót hoàn toàn, để lại mô bệnh tồn dư làm tăng nguy cơ tái phát tại chỗ.
Do đó buộc bệnh nhân phải trải qua phẫu thuật lần hai, một thủ thuật có tỷ lệ biến chứng cao hơn đáng kể so với lần mổ đầu tiên.
Mặt khác, sự không chắc chắn có thể khiến phẫu thuật viên quyết định nạo hạch cổ trung tâm dự phòng một cách thường quy.
Vì vậy đẩy những bệnh nhân có thể không hề có di căn vào các rủi ro phẫu thuật không cần thiết.
Đó là tổn thương thần kinh thanh quản quặt ngược gây thay đổi giọng nói hoặc liệt dây thanh và suy tuyến cận giáp dẫn đến hạ canxi máu có thể trở thành vĩnh viễn.
Không kịch bản nào thực sự phục vụ lợi ích tốt nhất cho bệnh nhân và chính sự mâu thuẫn lâm sàng này là điều mà các mô hình dự đoán dựa trên AI đang nỗ lực giải quyết.
Ví dụ: các bệnh viện lớn hàng năm tiếp nhận hàng nghìn ca ung thư tuyến giáp. Với tỷ lệ di căn hạch cao nhưng khả năng phát hiện qua siêu âm lại hạn chế.
Các bác sĩ thường phải đưa ra quyết định dựa trên kinh nghiệm lâm sàng nhiều hơn là bằng chứng hình ảnh rõ ràng.
Đây chính là khoảng trống mà AI có thể lấp đầy.
Các bằng chứng khoa học ủng hộ năng lực của AI trong giải quyết thách thức này rất thuyết phục.
Dữ liệu tổng hợp từ các phân tích gộp (meta-analysis) cho thấy hệ thống AI được huấn luyện trên dữ liệu siêu âm đạt độ nhạy 76% và độ đặc hiệu 78% trong dự đoán CLNM.
Nó vượt trội đáng kể so với kết quả của các bác sĩ chẩn đoán hình ảnh giàu kinh nghiệm khi sử dụng tiêu chí đánh giá thông thường.
Các kiến trúc học sâu (deep learning) thể hiện hiệu suất dự đoán vượt trội so với các phương pháp học máy truyền thống.
Kết quả tích cực nhờ khả năng trích xuất và tích hợp các đặc trưng hình ảnh phức tạp, đa chiều, những đặc trưng mà mắt người không thể nhận biết.
Hơn nữa, các nghiên cứu liên tục chứng minh những mô hình dự đoán mạnh mẽ nhất là các mô hình áp dụng phương pháp đa phương thức (multimodal), kết hợp đặc trưng hình ảnh siêu âm với các biến số lâm sàng như tuổi, giới tính và kích thước khối u nguyên phát.
Tích hợp nhiều nguồn dữ liệu đa dạng này phản ánh tư duy lâm sàng toàn diện vốn là đặc trưng của các chuyên gia y khoa dày dặn kinh nghiệm nhưng thực thi với mức độ nhất quán và khả năng mở rộng mà nhận thức con người khó có thể sánh được.
Bên cạnh đó, các mô hình AI dựa trên CT cũng cho kết quả ấn tượng.
Nó đạt độ nhạy 78% và độ đặc hiệu 89%, cung cấp dữ liệu bổ trợ có giá trị cao, hỗ trợ lập kế hoạch phẫu thuật cá thể hóa.
Từ đó giúp phẫu thuật viên đưa ra quyết định chính xác hơn về phạm vi nạo hạch cổ phù hợp.
Y học phân tử và phân tầng tiên lượng
Ngoài lĩnh vực chẩn đoán hình ảnh, AI đang tạo ra những đóng góp sâu sắc không kém trong hiểu rõ ung thư tuyến giáp ở cấp độ phân tử và hệ gen.
Đây là một bước chuyển đổi mô hình từ phân tích khối u trông như thế nào sang hiểu bản chất thực sự của khối u là gì.
Nó bao gồm hành vi sinh học, quỹ đạo tiến triển và khả năng đáp ứng với các chiến lược điều trị khác nhau.
Một bước tiến đột phá đáng chú ý là việc ứng dụng thuật toán
Chỉ dấu sinh học mạng lưới động (DNB – Dynamic Network Biomarker) để xác định các điểm chuyển tiếp then chốt trong quá trình tiến triển bệnh.
Nghiên cứu gần đây đã phát hiện một “điểm bùng phát” (tipping point) quan trọng xảy ra tại Giai đoạn II của ung thư tuyến giáp biệt hóa (DTC – Differentiated Thyroid Cancer).
Đó là nơi khối u trải qua sự chuyển đổi căn bản từ trạng thái sinh học tương đối ổn định sang trạng thái tiến triển với mức độ bất ổn phân tử tăng rõ rệt.
Phát hiện này có ý nghĩa vô cùng quan trọng vì nó gợi ý có tồn tại một cửa sổ thời gian hẹp nhưng có thể nhận diện được, trong đó quỹ đạo bệnh vẫn còn khả năng thay đổi nếu can thiệp kịp thời.
Khả năng phát hiện sự chuyển tiếp này trước khi nó biểu hiện trên lâm sàng đánh dấu một bước tiến đáng kể so với các hệ thống phân giai đoạn truyền thống.
Đó là những phương pháp chủ yếu dựa vào tiêu chí giải phẫu và thường không nắm bắt được các quá trình sinh học động đang thúc đẩy bệnh tiến triển.
Để dễ hình dung, có thể so sánh điều này với dự báo thời tiết.
Thay vì chỉ quan sát bầu trời để đoán mưa (giống như phân giai đoạn truyền thống dựa trên giải phẫu), DNB giống như theo dõi các chỉ số khí tượng ở cấp độ vi mô để phát hiện dấu hiệu bão sắp hình thành trước khi những đám mây đen xuất hiện trên bầu trời.
Dựa trên những thông tin cấp độ phân tử, các nhà nghiên cứu đã phát triển các công cụ phân tầng tinh vi.
Do đó giúp chuyển đổi dữ liệu hệ gen phức tạp thành thông tin lâm sàng có thể hành động ngay.
Hệ thống chấm điểm TCPSLevel giúp bác sĩ lâm sàng nhận diện những bệnh nhân có nguy cơ tiến triển bệnh cao, ngay cả khi các đánh giá lâm sàng và hình ảnh học thông thường cho thấy bệnh ở giai đoạn sớm, nguy cơ thấp.
Khả năng này giải quyết một trong những khía cạnh đáng lo ngại nhất trong quản lý ung thư tuyến giáp.
Đó là nhóm bệnh nhân có khối u tưởng chừng lành tính theo tiêu chí truyền thống nhưng cuối cùng lại diễn tiến hung hãn.
Bổ sung cho công cụ này, mô hình miniPC, một bộ phân loại được xây dựng dựa trên bảng gồm 12 gen sẽ phân nhóm bệnh nhân thành các phân nhóm phân tử riêng biệt.
Từ đó cung cấp nền tảng bằng chứng cần thiết cho những quyết định điều trị tinh tế hơn.
Phân tầng phân tử giúp bác sĩ lâm sàng xác định liệu bệnh nhân nên được theo dõi tích cực.
Đây là một phương pháp ngày càng được công nhận hiệu quả đối với bệnh nguy cơ thấp hay cần can thiệp phẫu thuật triệt để để ngăn chặn bệnh tiến triển.
Phân tích phân tử ứng dụng AI còn mở rộng đến con đường tín hiệu MAPK/ERK, một động lực trung tâm trong quá trình sinh ung thư tuyến giáp và cũng là đích điều trị quan trọng.
Thông qua nhận diện các mô hình biểu hiện bất thường ở những gen cụ thể như CCNA1, SFN và CDKN1C, phân tích hệ gen tăng cường bởi AI cải thiện đáng kể cả độ nhạy lẫn độ đặc hiệu trong việc phân biệt giữa các phân nhóm mô học.
Kết quả này đặc biệt rõ giữa ung thư tuyến giáp thể nhú (PTC – Papillary Thyroid Carcinoma) và ung thư tuyến giáp thể nang (FTC – Follicular Thyroid Carcinoma).
Khả năng phân biệt vốn rất khó thực hiện chính xác chỉ dựa trên xét nghiệm tế bào học đơn thuần có tác động trực tiếp đến kế hoạch phẫu thuật, quyết định điều trị iốt phóng xạ và chiến lược theo dõi dài hạn.
Tại nhiều nơi, nơi ung thư tuyến giáp có xu hướng gia tăng nhanh chóng, ứng dụng các công cụ phân tầng phân tử như TCPSLevel hay miniPC sẽ đặc biệt hữu ích trong việc tối ưu hóa nguồn lực y tế.
Do đó giúp tránh can thiệp quá mức ở bệnh nhân nguy cơ thấp, đồng thời không bỏ lỡ cơ hội điều trị sớm ở nhóm bệnh nhân có nguy cơ tiến triển cao.
Các ứng dụng nổi tiếng và phổ biến
Samsung S-Detect for Thyroid
Là một trong những giải pháp AI đầu tiên được ứng dụng trong thực hành lâm sàng, Samsung S-Detect đánh dấu bước ngoặt trong cách phần mềm thông minh kết hợp với thiết bị chẩn đoán hình ảnh.
Thay vì hoạt động như một nền tảng riêng biệt đòi hỏi bác sĩ phải xuất hình ảnh ra ngoài rồi thực hiện thêm nhiều bước xử lý, S-Detect vận hành trực tiếp bên trong các hệ thống siêu âm của Samsung như dòng RS85.
Nó đưa ra phân tích ngay tại thời điểm khám mà không làm gián đoạn quy trình quét.
Cách tiếp cận tích hợp này đặc biệt hữu ích tại các phòng khám có lưu lượng bệnh nhân lớn.
Đó là nơi mà mỗi bước thao tác thêm đều đồng nghĩa với thời gian chờ đợi kéo dài và năng suất khám giảm sút.
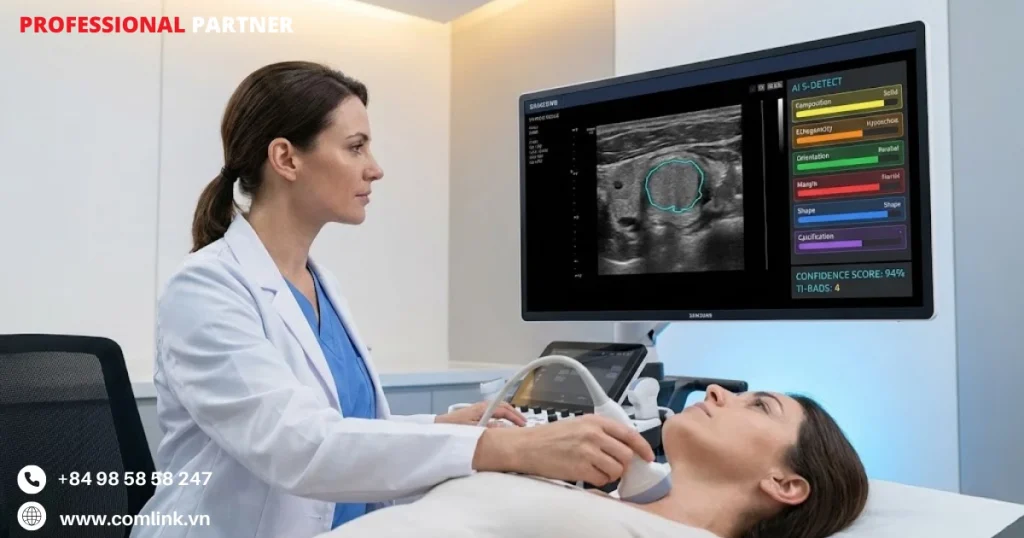
Hệ thống sử dụng mạng nơ-ron sâu để đánh giá sáu đặc điểm hình ảnh theo chuẩn từ vựng chẩn đoán theo thời gian thực:
- Thành phần cấu trúc.
- Độ hồi âm.
- Hướng phát triển.
- Đặc điểm bờ viền.
- Hình dạng.
- Sự hiện diện của các điểm vôi hóa.
Ngay khi bác sĩ xác định vùng cần quan tâm, S-Detect xử lý đồng thời tất cả các đặc điểm này và đưa ra khuyến nghị nhị phân là “Có thể lành tính” hoặc “Có thể ác tính.
Kết quả đầu ra ngắn gọn này đóng vai trò như một ý kiến tham khảo tức thì, giúp chuẩn hóa quá trình ra quyết định lâm sàng.
Ngoài ra, nền tảng hỗ trợ nhiều hướng dẫn phân loại quốc tế bao gồm ATA, BTA, EU-TIRADS, K-TIRADS và ACR-TIRADS.
Vì vậy đảm bảo báo cáo được thống nhất theo tiêu chuẩn toàn cầu bất kể vị trí địa lý.
Các nghiên cứu lâm sàng cho thấy S-Detect mang lại tác động lớn nhất đối với các bác sĩ ít kinh nghiệm, nâng độ chính xác chẩn đoán của họ từ 77,4% lên mức ấn tượng 89,6%.
Với các chuyên gia giàu kinh nghiệm, công cụ này chủ yếu đóng vai trò cơ chế xác nhận.
Do đó giúp giảm sự khác biệt giữa các bác sĩ khi đọc kết quả nên đảm bảo hai bác sĩ X-quang cùng khám một nhân tuyến giáp sẽ đi đến kết luận nhất quán.
Ví dụ: Tại các bệnh viện tuyến huyện, nơi bác sĩ siêu âm thường phải kiêm nhiệm nhiều chuyên khoa, S-Detect có thể đóng vai trò “người cố vấn số” giúp nâng cao chất lượng chẩn đoán tuyến giáp mà không cần chuyển bệnh nhân lên tuyến trên.
Koios DS Thyroid
Được phát triển bởi Koios Medical, nền tảng hỗ trợ quyết định lâm sàng này nổi bật nhờ cả tính linh hoạt trong triển khai lẫn quy mô dữ liệu huấn luyện khổng lồ.
Hệ thống có hai hình thức triển khai: dịch vụ đám mây hoặc tích hợp trực tiếp vào hạ tầng PACS hiện có.
Sự linh hoạt này đặc biệt quan trọng trong điều kiện y tế đa dạng từ các trung tâm y khoa học thuật lớn với hạ tầng máy chủ mạnh mẽ cho đến các phòng khám hình ảnh ngoại trú nhỏ hơn ưu tiên mô hình đám mây để giảm thiểu đầu tư phần cứng tại chỗ.
Điểm khác biệt về mặt kỹ thuật của Koios nằm ở nền tảng huấn luyện.
Thuật toán được phát triển dựa trên hơn hai triệu hình ảnh siêu âm thu thập từ mạng lưới 48 trung tâm trên toàn thế giới.
Sự đa dạng dữ liệu vượt trội đảm bảo hệ thống hoạt động tin cậy trên nhiều nhóm dân tộc khác nhau, các biến thể về thể trạng cơ thể cũng như các hãng sản xuất thiết bị siêu âm khác nhau.
Đây là một yếu tố then chốt mà nhiều công cụ AI có phạm vi hẹp hơn thường gặp khó khăn.
Hệ thống trích xuất tới 17.900 đặc trưng (feature) trên mỗi hình ảnh để tạo ra đánh giá nguy cơ ác tính, đồng bộ với cả hai hệ thống phân loại TI-RADS và BI-RADS.
Về hiệu quả kinh tế, Koios mang lại giá trị thuyết phục.
Các cơ sở y tế báo cáo giảm 35% số ca sinh thiết dương tính giả và cải thiện 30% năng suất hoạt động phòng khám.
Do đó dẫn đến tỷ suất hoàn vốn (ROI) từ 100% đến 400%.
Thêm vào đó, Koios giữ vị thế đặc biệt khi trở thành phần mềm AI tuyến giáp đầu tiên có lộ trình hoàn trả chi phí thông qua mã CPT Category 3 tại Hoa Kỳ.
Nó đã xóa bỏ rào cản lớn trong ứng dụng công nghệ khi đảm bảo nhà cung cấp dịch vụ y tế có thể thu hồi chi phí phân tích hỗ trợ bởi AI.
Ví dụ: Với bệnh viện đa khoa đang sử dụng hệ thống PACS tích hợp Koios qua đám mây là hoàn toàn khả thi mà không cần thay đổi hạ tầng CNTT hiện có.
Do đó giúp bệnh viện tiếp cận AI chẩn đoán mà không phải đầu tư thêm hàng tỷ đồng cho phần cứng chuyên dụng.
AmCAD-UT
Được phát triển bởi AmCad BioMed tại Đài Loan, AmCAD-UT giải quyết một trong những thách thức dai dẳng nhất của siêu âm: bản chất chủ quan vốn có trong việc đọc hình ảnh.
Hai bác sĩ X-quang giàu kinh nghiệm có thể cùng khám một nhân tuyến giáp nhưng bất đồng về việc nhân đó là giảm âm (hypoechoic) hay đồng âm (isoechoic), bờ viền không đều hay trơn nhẵn.
Đó là những khác biệt ảnh hưởng trực tiếp đến khuyến nghị điều trị.
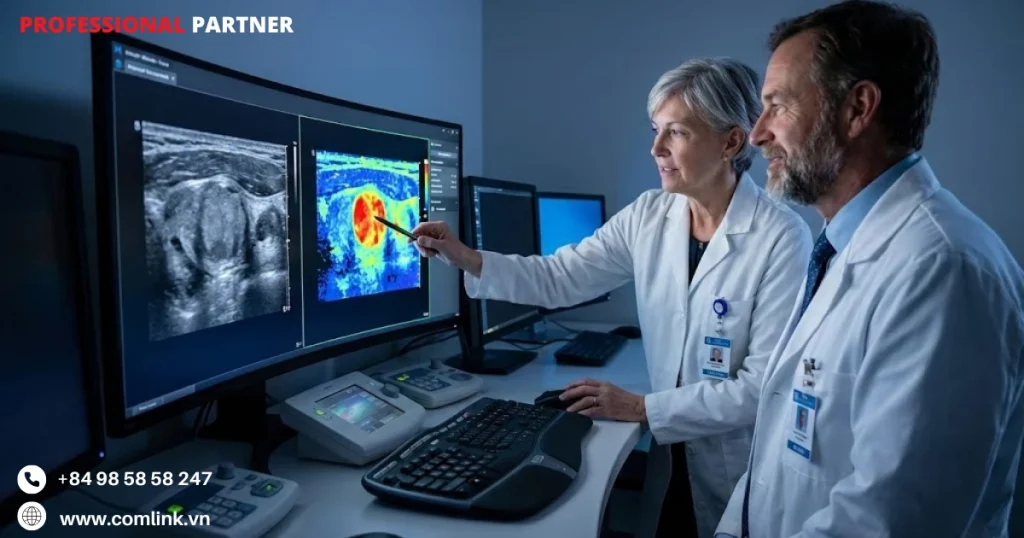
AmCAD-UT xử lý vấn đề này thông qua chuyển đổi các đặc điểm hình ảnh định tính thành bản đồ định lượng được mã hóa bằng màu sắc khi sử dụng công nghệ phân tích hình ảnh đã được cấp bằng sáng chế.
Phương pháp trực quan hóa biến các mẫu hình ảnh xám trừu tượng thành các lớp phủ màu trực quan, phân định rõ ràng mức độ hồi âm, bất thường bờ viền và các điểm vôi hóa.
Kết quả là một “ngôn ngữ hình ảnh chung” giúp giảm sự mơ hồ và tạo điều kiện cho các cuộc thảo luận lâm sàng hiệu quả hơn giữa các bác sĩ.
Dữ liệu hiệu suất cho thấy phương pháp định lượng tăng độ đặc hiệu lên 55% và độ nhạy lên 30% đối với các bác sĩ X-quang ít kinh nghiệm.
Do đó giảm đáng kể số ca phẫu thuật cắt tuyến giáp không cần thiết đối với nhân lành tính.
Đây là một cải thiện có ý nghĩa giúp bệnh nhân tránh được rủi ro phẫu thuật, thời gian hồi phục và phải dùng hormone thay thế suốt đời.
Nền tảng này cũng nổi bật với sự linh hoạt trong triển khai lâm sàng.
Nó hỗ trợ phân tích cả hình ảnh tĩnh lẫn video quét thời gian thực, tương thích với cả hệ điều hành Windows và Android.
Thiết kế đa nền tảng này giúp AmCAD-UT dễ dàng tiếp cận trong nhiều môi trường lâm sàng khác nhau, từ máy trạm bệnh viện đến cấu hình khám tại chỗ trên máy tính bảng.
Với xuất xứ từ Đài Loan là thị trường có nhiều điểm tương đồng với Việt Nam về cấu trúc hệ thống y tế, AmCAD-UT có lợi thế để thích ứng với các nước Châu Á.
Khả năng chạy trên máy tính bảng Android đặc biệt phù hợp với các phòng khám tư nhân tại Việt Nam, nơi chi phí đầu tư thiết bị luôn là yếu tố cân nhắc hàng đầu.
See-Mode Technologies
Trong khi hầu hết các công cụ AI tuyến giáp tập trung vào mô tả đặc điểm nhân mà bác sĩ đã xác định trước, See-Mode Technologies mở rộng phạm vi tự động hóa bao trùm toàn bộ quy trình chẩn đoán.
Nền tảng này nắm giữ vị thế pháp lý khi trở thành giải pháp đầu tiên được FDA cấp phép cho cả Phát hiện có Hỗ trợ Máy tính (Computer-Aided Detection – CADe) và Chẩn đoán có Hỗ trợ Máy tính (Computer-Aided Diagnosis – CADx) đối với nhân tuyến giáp.
Ý nghĩa thực tiễn khi được cấp phép kép vô cùng giá trị.
Hệ thống không chỉ phân loại nhân được đưa vào phân tích mà còn chủ động phát hiện những nhân mà bác sĩ có thể bỏ sót đặc biệt trong các trường hợp đa nhân phức tạp, nơi những tổn thương nhỏ hơn dễ bị che khuất bởi các khối u chiếm ưu thế.
Hệ thống tự động phát hiện nhân trong cả hình ảnh đơn nhân và đa nhân mà không cần thao tác thủ công như đánh dấu vùng quan tâm.
Khả năng phát hiện tự động “rảnh tay” đặc biệt giá trị trong các tình huống tầm soát lưu lượng lớn.
Đó là những nơi sự mệt mỏi của bác sĩ có thể ảnh hưởng đến khả năng chú ý đến những phát hiện tinh vi.
Hơn nữa, See-Mode tự động tạo bản nháp báo cáo được điền sẵn điểm đánh giá TIRADS và số đo nhân.
Do đó chuyển đổi quy trình làm tài liệu từ nhập liệu thủ công sang quy trình “xem lại và phê duyệt.”
Nhờ loại bỏ công đoạn soạn báo cáo tốn nhiều thời gian, See-Mode giúp bác sĩ X-quang tập trung nguồn lực trí tuệ vào phán đoán lâm sàng và giao tiếp với bệnh nhân, những lĩnh vực mà chuyên môn con người vẫn không thể thay thế.
Ví dụ: Trong một ca siêu âm tuyến giáp thông thường, bác sĩ có thể phát hiện 2-3 nhân lớn nhưng bỏ qua 1 nhân nhỏ ẩn phía sau. See-Mode đóng vai trò như “đôi mắt thứ hai” không biết mệt mỏi, quét toàn bộ hình ảnh và đánh dấu mọi nhân nghi ngờ.
Vì thế giảm đáng kể nguy cơ bỏ sót tổn thương, đặc biệt vào cuối ca trực khi sự tập trung của bác sĩ suy giảm.
MEDO-Thyroid
Với cách tiếp cận khác biệt hoàn toàn so với các đối thủ, MEDO-Thyroid tái định nghĩa chính quy trình thu nhận hình ảnh siêu âm thay vì chỉ phân tích hình ảnh đã chụp theo cách truyền thống.
Siêu âm tuyến giáp thông thường đòi hỏi người thao tác phải chụp các hình ảnh tĩnh với hướng chính xác.
Khi đó phải đáp ứng tiêu chuẩn chất lượng nhất định, một kỹ năng cần đào tạo và kinh nghiệm đáng kể.
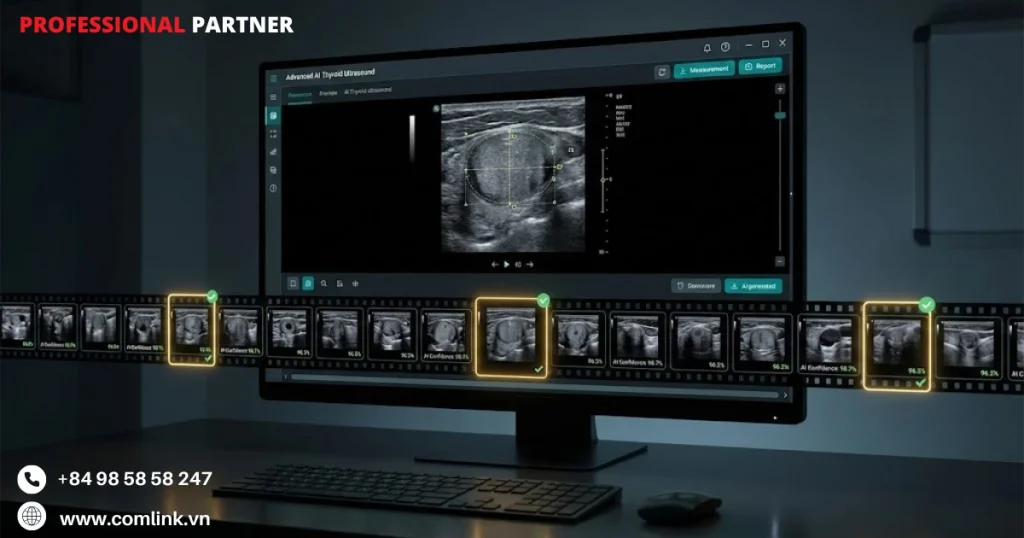
MEDO-Thyroid xóa bỏ rào cản này khi chấp nhận các đoạn quét video đơn giản qua vùng tuyến giáp.
Sau đó AI tự động chọn ra những khung hình tối ưu nhất phục vụ phân tích và đo lường.
Cách tiếp cận dựa trên video mang lại tác động sâu rộng đối với khả năng tiếp cận dịch vụ y tế.
Trong các môi trường y tế từ xa, phòng khám vùng nông thôn hoặc những nơi không có kỹ thuật viên siêu âm được đào tạo bài bản, một nhân viên y tế chỉ cần qua huấn luyện siêu âm cơ bản vẫn có thể thực hiện thao tác quét.
Thuật toán của MEDO đảm nhận các nhiệm vụ phức tạp như chọn khung hình, phát hiện nhân và đo lường.
Hệ thống tự động tính toán kích thước thùy tuyến giáp và eo tuyến giáp, xác định vị trí nhân và mô tả đặc điểm phát hiện theo hệ thống phân loại TI-RADS.
Nhờ hạ thấp ngưỡng kỹ năng cần thiết để thực hiện đánh giá tuyến giáp chất lượng, MEDO-Thyroid có tiềm năng mở rộng đáng kể khả năng tầm soát tại các cộng đồng thiếu nguồn lực y tế.
Đó là nơi tình trạng thiếu hụt chuyên gia hiện đang hạn chế việc phát hiện sớm ung thư tuyến giáp.
Ví dụ: Tại các trạm y tế xã vùng núi, nơi bác sĩ chuyên khoa nội tiết gần như không có, MEDO-Thyroid mở ra khả năng tầm soát tuyến giáp qua các chương trình khám sức khỏe lưu động.
Nhân viên y tế chỉ cần quét đầu dò qua cổ bệnh nhân, AI sẽ tự động phân tích và gửi kết quả về bệnh viện tuyến trên để bác sĩ chuyên khoa xem xét từ xa.
Có thể bạn quan tâm

Liên hệ

Địa chỉ
Tầng 3 Toà nhà VNCC
243A Đê La Thành Str
Q. Đống Đa-TP. Hà Nội

info@comlink.com.vn

Phone
+84 98 58 58 247











