

Ứng dụng AI cho ung thư bàng quang là gì
Ứng dụng AI cho ung thư bàng quang là sử dụng công nghệ và thuật toán AI để phát hiện các tổn thương phẳng tinh vi qua nội soi nâng cao, phân độ ác tính chính xác qua giải phẫu bệnh kỹ thuật số, dự báo rủi ro tái phát và đáp ứng thuốc cá thể hóa.
Vì vậy ứng dụng AI cho ung thư bàng quang không chỉ dừng lại ở các phần mềm hỗ trợ chẩn đoán hình ảnh mà còn mở rộng ra toàn bộ quy trình để tăng độ chính xác chẩn đoán, điều chỉnh phương pháp điều trị cho từng bệnh nhân, theo dõi tình trạng bệnh hiệu quả hơn và cuối cùng là nâng cao kết quả điều trị cho bệnh nhân.
Nội soi bàng quang
Tăng cường khả năng phát hiện tổn thương
Một trong những thách thức dai dẳng nhất trong nội soi bàng quang là phát hiện các tổn thương có độ tương phản thị giác rất thấp so với mô lành xung quanh.
Ung thư biểu mô tại chỗ (CIS) là một dạng ung thư bàng quang không xâm lấn cơ, độ ác tính cao đặc biệt khó nhận diện.
Nó chỉ biểu hiện dưới dạng các vùng đỏ nhẹ trên niêm mạc, dễ bị nhầm lẫn với các tình trạng viêm lành tính như viêm bàng quang.
Bỏ sót CIS trong quá trình nội soi có thể dẫn đến hậu quả lâm sàng nghiêm trọng, khi khối u âm thầm tiến triển xâm lấn lớp cơ trước khi được chẩn đoán đúng.
Các mô hình học sâu tích hợp trực tiếp vào hệ thống video nội soi xử lý luồng dữ liệu hình ảnh theo thời gian thực với độ chi tiết vượt xa khả năng tri giác của con người.
AI phân tích từng khung hình để tìm kiếm các dấu hiệu hình thái học bao gồm bất thường mạch máu, kết cấu niêm mạc không đều và sai lệch màu sắc tinh tế.
Sau đó tạo ra bản đồ nhiệt (heatmap) hoặc khung đánh dấu vùng bất thường hiển thị trực tiếp trên màn hình nội soi.
Hệ thống hỗ trợ thị giác liên tục thu hút sự chú ý của bác sĩ tiết niệu đến các vùng đáng ngờ, hoạt động như một cặp mắt thứ hai không bao giờ mỏi mệt hay mất tập trung.
Công nghệ này đặc biệt có giá trị trong các đơn vị nội soi khối lượng lớn, nơi sự mệt mỏi của bác sĩ có thể làm giảm sự cảnh giác chẩn đoán trong các ca thủ thuật kéo dài.
Ví dụ: Tại một bệnh viện ung bướu lớn, bác sĩ nội soi thực hiện hàng chục ca mỗi ngày. Đến ca thứ 15 trong buổi chiều, khả năng tập trung giảm đáng kể.
Hệ thống AI lúc này đóng vai trò như một trợ lý “không biết mệt”, tự động đánh dấu một vùng niêm mạc đỏ nhạt ở góc bàng quang mà bác sĩ có thể đã lướt qua.
Kết quả sinh thiết sau đó xác nhận đây là CIS giai đoạn sớm.
Ngoài khả năng phát hiện, AI còn thể hiện năng lực phân loại hình thái học tinh vi.
Chúng có khả năng phân loại các tổn thương đã xác định thành dạng nhú (papillary), dạng phẳng (flat) hoặc hỗn hợp ngay trong thời gian thực.
Khả năng phân loại có tác động trực tiếp đến phẫu thuật.
Khi bác sĩ tiết niệu thực hiện cắt u bàng quang qua nội soi niệu đạo (TURBT) nhận được đánh giá hình thái học từ AI trước khi cắt bỏ nên lên kế hoạch phẫu thuật trở nên có định hướng hơn rõ rệt.
Tổn thương dạng phẳng đòi hỏi diện cắt rộng hơn so với u dạng nhú.
Khi biết trước điều này giúp phẫu thuật viên đảm bảo lấy sạch toàn bộ mô có khả năng ác tính trong một lần phẫu thuật duy nhất.
Vì vậy giảm nguy cơ tái phát và tránh cho bệnh nhân phải trải qua nhiều lần can thiệp lặp đi lặp lại.
Giảm thiểu sai lệch giữa các bác sỹ
Nội soi bàng quang truyền thống về bản chất luôn tiềm ẩn sự biến thiên trong kết quả và được thừa nhận rộng rãi trong cộng đồng tiết niệu học.
Diễn giải các tổn thương ranh giới phụ thuộc nhiều vào nền tảng đào tạo của từng bác sĩ, kinh nghiệm lâm sàng tích lũy và thậm chí cả mức độ mệt mỏi tại thời điểm khám.
Sự không nhất quán đặc biệt rõ nét giữa các cơ sở y tế khác nhau.
Khi một tổn thương được đánh giá là đáng ngờ tại trung tâm ung bướu tuyến trên có thể bị bỏ qua như một tình trạng lành tính tại bệnh viện tuyến dưới thiếu chuyên khoa sâu.
Với bệnh nhân, sự không đồng nhất trực tiếp dẫn đến bất bình đẳng trong khả năng tiếp cận chẩn đoán chính xác và kịp thời.
Nội soi bàng quang hỗ trợ AI giải quyết bất cập hệ thống này bằng cách đưa vào một tiêu chuẩn đánh giá khách quan vì có thể tái lập, hoạt động độc lập với phán đoán chủ quan của từng bác sĩ.
Các hệ thống AI được huấn luyện trên bộ dữ liệu tuyển chọn gồm hàng chục nghìn hình ảnh nội soi có chú thích, lấy từ nhiều nhóm bệnh nhân và nguồn cơ sở y tế đa dạng.
Do đó giúp chúng nhận diện được phổ rộng các dạng tổn thương kể cả những trường hợp không điển hình hoặc mơ hồ vốn thách thức ngay cả các chuyên gia dày dạn kinh nghiệm.
Trong các nghiên cứu so sánh có kiểm soát, mô hình AI đã chứng minh độ chính xác chẩn đoán tương đương và trong một số tình huống khó đặc biệt, còn vượt trội hơn so với các chuyên gia đầu ngành.
Điều này đặc biệt quan trọng trong phát hiện tổn thương phẳng, không dạng nhú, vốn có mức độ đồng thuận giữa các bác sĩ trong lịch sử luôn thấp.
Ví dụ: Chênh lệch chuyên môn giữa bệnh viện thành phố lớn với các bệnh viện đa khoa tỉnh là điều không thể phủ nhận.
Một hệ thống AI nội soi chuẩn hóa đặt tại bệnh viện tỉnh sẽ giúp bác sĩ địa phương đưa ra đánh giá có chất lượng tương đương với bác sĩ chuyên khoa sâu ở tuyến trung ương.
Do đó rút ngắn con đường đến với chẩn đoán đúng cho bệnh nhân ở vùng xa.
Hiệu ứng chuẩn hóa của AI đặc biệt quý giá tại các cơ sở y tế hạn chế nguồn lực hoặc ở vùng địa lý xa xôi.
Một bác sĩ tiết niệu tuyến huyện được hỗ trợ bởi trợ lý AI có thể cung cấp mức độ nhất quán trong chẩn đoán mà trước đây chỉ có tại các trung tâm y tế học thuật lớn.
Hơn nữa, các hệ thống AI còn tạo ra hồ sơ quyết định có thể kiểm tra ghi lại các vùng được đánh dấu và điểm độ tin cậy tương ứng, hỗ trợ quy trình đảm bảo chất lượng và xem xét hồi cứu ca bệnh.
Kết quả là một hệ sinh thái chẩn đoán công bằng hơn, trong đó mọi bệnh nhân dù được chăm sóc ở đâu đều được hưởng cùng một mức độ phân tích tương đương.
Đây là bước tiến đo lường được để thu hẹp khoảng cách giữa ung thư học thực hành tốt nhất và thực tế lâm sàng thường ngày.
Chẩn đoán hình ảnh không xâm lấn
Phân tầng giai đoạn và dự báo xâm lấn cơ
Một trong những quyết định quan trọng nhất trong điều trị ung thư bàng quang là xác định liệu khối u có xâm lấn vào lớp cơ chóp bàng quang hay chưa.
Đây chính là ranh giới phân biệt giữa ung thư bàng quang chưa xâm lấn cơ (NMIBC) và ung thư bàng quang đã xâm lấn cơ (MIBC).
Chỉ một sự khác biệt này đã trực tiếp quyết định bệnh nhân sẽ được điều trị bảo tồn bàng quang hay phải phẫu thuật cắt bỏ bàng quang toàn phần.
Do đó phân giai đoạn chính xác không chỉ đơn thuần là một nhiệm vụ chẩn đoán mà còn là quyết định lâm sàng có thể thay đổi cả cuộc đời người bệnh.
Đánh giá trễ hoặc không chính xác mức độ xâm lấn cơ có thể dẫn đến hai hậu quả nguy hiểm:
- Điều trị không đủ liều để ung thư xâm lấn tiếp tục tiến triển.
- Phẫu thuật triệt căn không cần thiết làm giảm vĩnh viễn chất lượng sống của bệnh nhân.
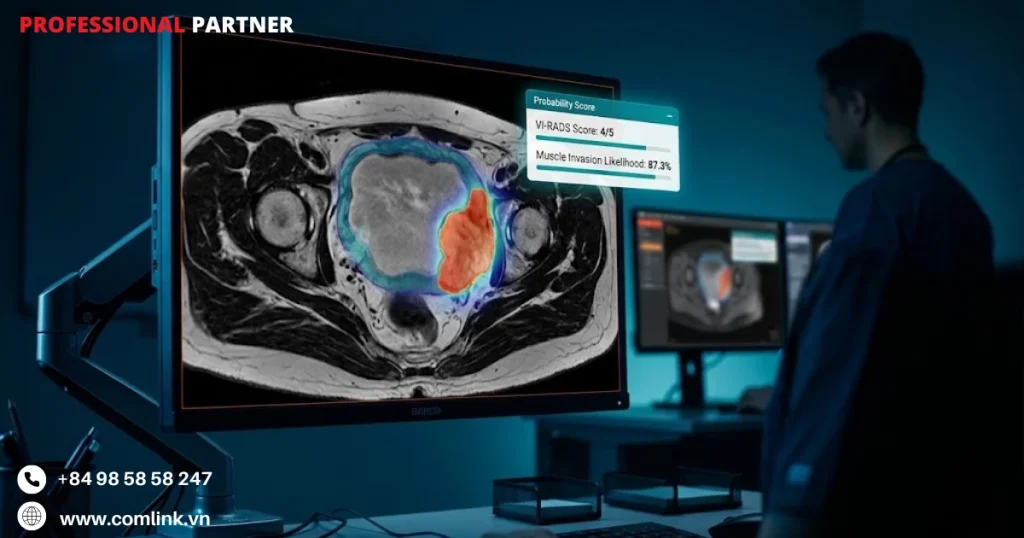
AI giải quyết thách thức này bằng cách phân tích các đặc trưng Phóng xạ học (Radiomics) phức tạp được trích xuất từ ảnh MRI, thường được diễn giải thông qua hệ thống phân loại chuẩn hóa VI-RADS.
Radiomics là phương pháp định lượng và trích xuất một lượng lớn đặc trưng hình ảnh bao gồm kết cấu mô, hình dạng và phân bố cường độ tín hiệu.
Đây là những yếu tố vô hình với mắt thường nhưng chứa đựng thông tin chẩn đoán có giá trị cao.
Các mô hình AI xử lý có hệ thống tập hợp đặc trưng đa chiều để đưa ra dự đoán xác suất về mức độ xâm lấn cơ với độ nhất quán vượt trội so với cách đọc hình ảnh trực quan thông thường của bác sĩ chẩn đoán hình ảnh.
Ví dụ: Tại bệnh viện, khi một bệnh nhân nam 58 tuổi có khối u bàng quang phát hiện qua nội soi.
Thay vì chỉ dựa vào đánh giá chủ quan của bác sĩ đọc MRI, hệ thống AI phân tích Radiomics có thể tự động chấm điểm VI-RADS từ 1–5 trong vài phút.
Do đó giúp hội đồng điều trị quyết định ngay liệu bệnh nhân cần cắt bỏ u qua nội soi (TURBT) hay tiến thẳng đến hóa trị tân hỗ trợ trước mổ cắt bàng quang.
Một bước phát triển đặc biệt sáng tạo trong lĩnh vực này là Chỉ số Giai đoạn Kết hợp, một mô hình AI được huấn luyện trên các đặc trưng Radiomics nhằm phân loại bệnh nhân vào giai đoạn T2 trở lên.
Đây là ngưỡng mà tại đó hóa trị tân hỗ trợ trở nên phù hợp về mặt lâm sàng.
Khả năng này đặc biệt quan trọng trong tối ưu hóa lựa chọn bệnh nhân trước khi lập kế hoạch phẫu thuật.
Do đó đảm bảo những người thực sự có thể hưởng lợi từ hóa trị tiền phẫu được tiếp cận điều trị kịp thời.
Kết quả là một lộ trình điều trị cá thể hóa, có cơ sở bằng chứng, giúp giảm cả tình trạng điều trị quá mức lẫn điều trị chưa đủ.
Từ đó trực tiếp cải thiện tỷ lệ sống sót và tối ưu hóa nguồn lực tại các khoa ung bướu.
Tối ưu hóa chất lượng hình ảnh và giảm liều tia X
Quản lý ung thư bàng quang thường đòi hỏi theo dõi hình ảnh định kỳ nhiều lần.
Đó là yêu cầu lâm sàng tất yếu nhưng kèm theo gánh nặng bức xạ tích lũy đáng kể.
Bệnh nhân theo dõi lâu dài có thể phải chụp CT nhiều lần trong suốt nhiều tháng hoặc nhiều năm.
Vì vậy mức phơi nhiễm bức xạ tích lũy từ các phác đồ liều cao thông thường là một nguy cơ sức khỏe thực sự, có thể đo lường được.
Do đó tối ưu hóa hình ảnh bằng AI không chỉ là một cải tiến kỹ thuật đơn thuần, mà là một biện pháp can thiệp bảo vệ bệnh nhân.
Ngoài ra còn giúp các bác sĩ duy trì độ chính xác chẩn đoán trong khi giảm thiểu có hệ thống tác hại từ bức xạ.
Các thuật toán AI ứng dụng trong chụp CT thực hiện tái tạo và nâng cao hình ảnh theo thời gian thực, tận dụng kỹ thuật học sâu để khử nhiễu và làm sắc nét độ phân giải giải phẫu ngay cả khi ảnh được chụp theo giao thức liều thấp.
Những mô hình sử dụng tái tạo lặp hay khử nhiễu bằng mạng nơ-ron sâu có thể bù đắp cho tín hiệu yếu vốn có trong các lần chụp liều thấp.
Sau đó khôi phục độ rõ nét của hình ảnh đến mức tương đương với ảnh chụp liều đầy đủ.
Nhờ đó, các tổn thương nhỏ ở bàng quang, hiện tượng dày thành bàng quang hay các thay đổi giai đoạn đầu vẫn hiện thị rõ ràng với bác sĩ đọc hình ảnh.
Ví dụ: Một bệnh nhân 45 tuổi sau phẫu thuật TURBT cần theo dõi CT định kỳ mỗi 3 tháng trong 2 năm với tổng cộng 8 lần chụp.
Với CT liều thông thường, tổng liều bức xạ tích lũy có thể vượt ngưỡng an toàn khuyến cáo.
Nhờ AI tái tạo hình ảnh liều thấp, mỗi lần chụp chỉ dùng 30–40% liều bức xạ ban đầu, trong khi chất lượng ảnh vẫn đủ để phát hiện tái phát khối u kích thước dưới 5mm.
Ý nghĩa thực tiễn đặc biệt có lợi cho những bệnh nhân đang trong giai đoạn theo dõi tích cực sau cắt bỏ u bàng quang qua nội soi (TURBT) hoặc đang trong phác đồ chờ theo dõi.
Với CT liều thấp có hỗ trợ AI, các bác sĩ lâm sàng có thể lên lịch theo dõi với tần suất dày hơn mà không làm tăng nguy cơ bức xạ tích lũy, điều mà trước đây rất khó thực hiện.
Tích hợp liền mạch AI vào quy trình CT hiện có cũng đồng nghĩa với việc kỹ thuật viên chẩn đoán hình ảnh và bác sĩ X-quang gần như không bị gián đoạn quy trình làm việc, trong khi độ tự tin chẩn đoán được nâng cao đáng kể.
Vì thế kết quả cuối cùng là phát hiện tái phát sớm hơn và can thiệp lâm sàng kịp thời hơn.
Giải phẫu bệnh kỹ thuật số và phân độ ác tính
Mô hình ShuffleNet
Trong ung thư học hiện đại, phân loại độ ác tính khối u chính xác không đơn thuần là bài toán học thuật mà là nền tảng lâm sàng quyết định toàn bộ phác đồ điều trị.
Với bệnh nhân ung thư bàng quang không xâm lấn cơ (NMIBC), ranh giới giữa phân loại độ thấp và độ cao có thể là sự khác biệt giữa theo dõi định kỳ và hóa trị nội bàng quang tích cực.
Tuy nhiên phương pháp phân loại truyền thống vẫn chịu sự biến động đáng kể giữa các bác sĩ giải phẫu bệnh.
Các nghiên cứu cho thấy tỷ lệ bất đồng có thể lên tới 30% khi đánh giá các trường hợp ranh giới trong khi yêu cầu về độ chính xác chẩn đoán chưa bao giờ cao như lúc này.
Mô hình ShuffleNet ra đời để giải quyết thách thức đó, dựa trên kiến trúc mạng nơ-ron tích chập (CNN) đa tỉ lệ dạng kim tự tháp.
Nó thiết kế mô phỏng cách các bác sĩ giải phẫu bệnh có kinh nghiệm thực sự quan sát mô bệnh học.
Đầu tiên nhìn tổng thể cấu trúc mô, sau đó phóng to để phân tích từng chi tiết tế bào.
ShuffleNet đồng thời phân tích các đặc điểm bệnh lý cục bộ như độ loạn nhân, phân bố chất nhiễm sắc, và hình ảnh phân bào song song với kiến trúc mô tổng thể, bao gồm cấu trúc nhú và sự phân lớp của tế bào biểu mô đường tiết niệu.
Toàn bộ dữ liệu này được trích xuất từ ảnh tiêu bản kỹ thuật số độ phân giải cao (WSI) là loại tiêu bản giải phẫu bệnh số hóa có thể phân tích ở mức độ phóng đại mà mắt thường không thể đạt được.
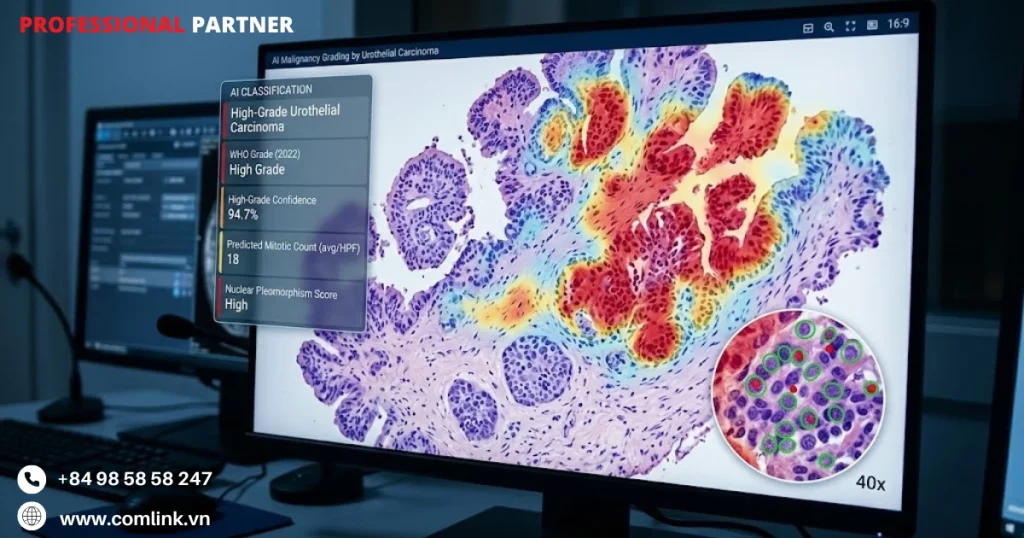
Qua kiểm định lâm sàng nghiêm ngặt, ShuffleNet đạt độ chính xác chẩn đoán 94,25%, độ nhạy 94,47% và độ đặc hiệu 94,03% ngang tầm với bác sĩ giải phẫu bệnh chuyên gia.
Điểm đáng chú ý là khả năng tuân thủ tiêu chuẩn WHO trong việc xác định ngưỡng định lượng của ShuffleNet.
Theo hướng dẫn phân loại của WHO, một khối u chỉ được xếp vào độ cao khi hơn 5% diện tích tiêu bản có biểu hiện đặc trưng của tế bào ác tính độ cao.
Chỉ số ngưỡng này cực kỳ khó ước lượng bằng mắt một cách nhất quán.
ShuffleNet đo lường diện tích bề mặt đó với độ chính xác tính toán, giảm đáng kể sai sót phân loại ở vùng ranh giới mập mờ giữa độ thấp và độ cao.
Với người bệnh, điều này mang lại chẩn đoán đáng tin cậy hơn, cường độ điều trị phù hợp hơn và giảm thiểu nguy cơ điều trị quá mức hoặc bỏ sót giai đoạn bệnh nguy hiểm.
Tối ưu hóa quy trình làm việc
Ngoài độ chính xác chẩn đoán, một trong những thách thức cấp thiết nhất của giải phẫu bệnh hiện đại là năng lực hệ thống.
Khối lượng tiêu bản cần được chuyên gia đọc ngày càng vượt xa số lượng bác sĩ giải phẫu bệnh tiết niệu có sẵn trên toàn cầu.
Tại các trung tâm ung bướu lớn, một bác sĩ có thể phải đọc hàng chục mẫu sinh thiết bàng quang mỗi ngày, mỗi mẫu đòi hỏi kiểm tra cẩn thận ở nhiều mức độ phóng đại khác nhau.
Gánh nặng công việc này không chỉ làm tăng nguy cơ sai sót do mệt mỏi mà còn gây chậm trễ đáng kể trong thời gian trả kết quả nên ảnh hưởng trực tiếp đến tiến độ lập kế hoạch điều trị.
Hệ thống sàng lọc sơ bộ bằng AI mở ra một hướng tiếp cận hoàn toàn mới trong quản lý quy trình giải phẫu bệnh.
Thay vì thay thế bác sĩ, các hệ thống này đóng vai trò như một lớp phân loại thông minh.
Chúng tự động duyệt hàng trăm tiêu bản số hóa, áp dụng thuật toán phân loại đã được huấn luyện để nhận diện các mẫu có đặc điểm ác tính, rồi đưa các ca ưu tiên lên trước để chuyên gia xem xét ngay lập tức.
Cơ chế xếp hàng thông minh đảm bảo bác sĩ tập trung sự chú ý cao nhất vào những ca thực sự cần thiết, trong khi các tiêu bản thông thường hoặc rõ ràng lành tính được xử lý hiệu quả hơn.
Trong các triển khai lâm sàng thực tế, sàng lọc sơ bộ bằng AI đã rút ngắn thời gian đọc tiêu bản trung bình từ khoảng 17 phút xuống còn 8,5 phút nên giảm tới 54,83% mà không ảnh hưởng đến độ chính xác chẩn đoán.
Tỷ lệ hiệu suất này thực chất nhân đôi năng lực chẩn đoán của một khoa giải phẫu bệnh mà không cần bổ sung nhân lực.
Tác động không chỉ dừng lại ở các con số hiệu suất tại các bệnh viện lớn ở đô thị.
Tại vùng nông thôn, khu vực thu nhập thấp và các nước đang phát triển nơi bác sĩ giải phẫu bệnh tiết niệu chuyên sâu cực kỳ thiếu hụt.
Khi đó hệ thống sàng lọc AI đóng vai trò cân bằng hóa trong cung ứng dịch vụ y tế.
Một bệnh viện tuyến huyện với năng lực giải phẫu bệnh hạn chế hoàn toàn có thể ứng dụng giải phẫu bệnh kỹ thuật số hỗ trợ AI để đạt tiêu chuẩn chẩn đoán vốn chỉ có ở các trung tâm y tế lớn.
Khả năng này đặc biệt có ý nghĩa với các quốc gia Đông Nam Á, châu Phi hạ Sahara và Mỹ Latinh, nơi gánh nặng ung thư bàng quang đang gia tăng trong khi khoảng trống chuyên gia vẫn còn rất lớn.
Đây chính là một trong những lợi ích lâu dài sâu sắc nhất khi tích hợp AI vào giải phẫu bệnh ung thư học.
Cá thể hóa điều trị và dự đoán đáp ứng
Từ thống kê quần thể đến dự báo cá nhân hóa
Một trong những rào cản lớn nhất trong điều trị ung thư bàng quang xâm lấn cơ (MIBC) là tính khó lường của phác đồ hóa trị bổ trợ trước phẫu thuật dựa trên cisplatin, tiêu chuẩn vàng hiện hành trong quản lý MIBC.
Dù được sử dụng rộng rãi, chỉ khoảng một phần ba bệnh nhân đạt được đáp ứng bệnh lý hoàn toàn.
Vì vậy phần lớn phải chịu độc tính và trì hoãn điều trị mà không thu được lợi ích thực sự.
Khoảng trống điều trị này đặt ra cái giá lâm sàng đắt đỏ vì trì hoãn phẫu thuật ở những bệnh nhân không đáp ứng có thể ảnh hưởng nghiêm trọng đến kết quả sống còn, trong khi người bệnh vẫn phải gánh chịu các tác dụng phụ hoàn toàn có thể tránh được.
Vì vậy, xác định trước bệnh nhân nào sẽ đáp ứng điều trị không đơn thuần là bài toán học thuật mà đây là yêu cầu thiết yếu về an toàn bệnh nhân và chất lượng cuộc sống.
Để giải quyết thách thức này, các nhà nghiên cứu tại Weill Cornell Medicine đã phát triển một mô hình đột phá ứng dụng Mạng Nơ-ron Đồ thị (GNN) kiến trúc học sâu được thiết kế đặc biệt để phân tích dữ liệu quan hệ.
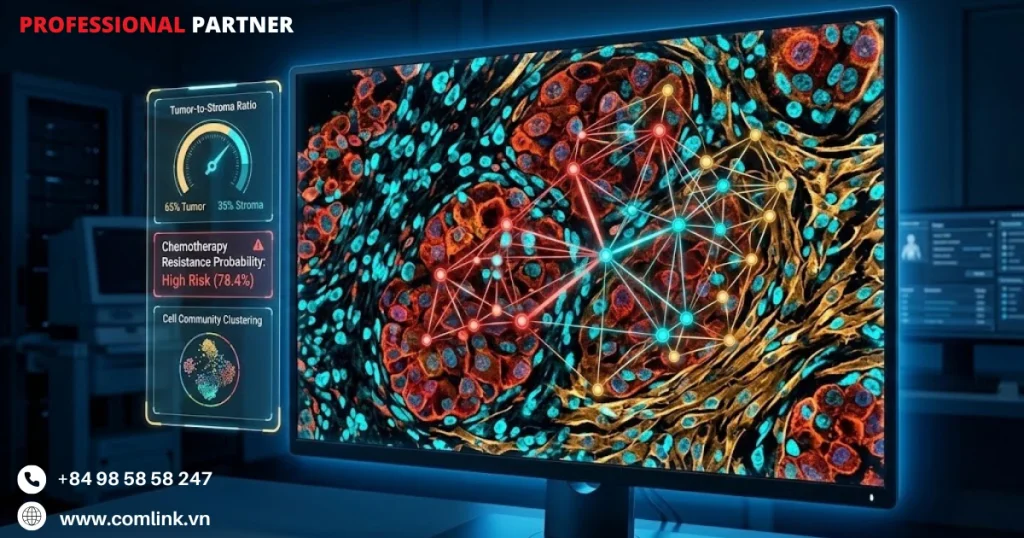
Khác với phân tích hình ảnh thông thường vốn xem xét từng tế bào riêng lẻ, mô hình dựa trên GNN lập bản đồ tương tác không gian giữa tế bào khối u, tế bào miễn dịch và nguyên bào sợi liên quan đến ung thư trong vi môi trường khối u.
Mô hình ghi lại cách các cộng đồng tế bào này giao tiếp và cạnh tranh với nhau.
Từ đó tiết lộ tỷ lệ giữa tế bào khối u ác tính và các thành phần mô đệm như nguyên bào sợi là yếu tố dự báo đáng tin cậy về tình trạng kháng hóa trị.
Phân tích tương tác đa bào này biến dữ liệu tĩnh từ tiêu bản mô thành thông tin sinh học động.
Ví dụ: Thay vì chỉ nhìn vào từng “nhân vật” trong khối u, GNN quan sát cả “mạng lưới quan hệ” giữa chúng.
Chức năng này tương tự như phân tích mạng xã hội để hiểu ai ảnh hưởng đến ai, từ đó dự báo hướng phát triển của toàn bộ hệ thống.
Bác sĩ ung thư học nay có thể phân tầng bệnh nhân MIBC trước khi bắt đầu hóa trị bổ trợ để hướng những bệnh nhân có khả năng không đáp ứng sang các phác đồ thay thế hoặc lên kế hoạch phẫu thuật sớm hơn.
Sau đó giúp những bệnh nhân thực sự đáp ứng không bị trì hoãn điều trị không cần thiết.
Điều này đặc biệt có giá trị với những bệnh nhân có thể trạng ở ngưỡng ranh giới.
Đó là khi tránh các chu kỳ hóa trị không hiệu quả có thể bảo tồn đáng kể năng lực chức năng trước khi cắt bàng quang.
Dự đoán đáp ứng liệu pháp miễn dịch bằng AI
Với bệnh nhân ung thư bàng quang là ứng viên tiềm năng cho liệu pháp ức chế điểm kiểm soát miễn dịch
Pembrolizumab, thuốc kháng PD-1 đã được phê duyệt cho cả ung thư di căn lẫn NMIBC không đáp ứng BCG nên xác định ai thực sự được hưởng lợi từ liệu pháp miễn dịch vẫn còn là bài toán nan giải.
Tiêu chí lựa chọn thông thường phụ thuộc nhiều vào biểu hiện PD-L1 và Gánh nặng Đột biến Khối u (TMB) nhưng các phương pháp dựa trên dấu ấn sinh học đơn lẻ này có những giới hạn dự báo đáng kể.
Ví dụ: biểu hiện PD-L1 không đồng nhất giữa các vùng khác nhau của khối u và dao động theo phác đồ điều trị trước đó, khiến nó không đủ tin cậy khi đứng một mình trong dự báo hiệu quả liệu pháp miễn dịch.
AI đưa ra một khung dự báo toàn diện hơn bằng cách kết hợp Phân tích Radiomics trích xuất các đặc trưng định lượng đa chiều từ hình ảnh y tế với dữ liệu hệ gen và phân tử.
Chữ ký Radiomics từ ảnh CT hoặc MRI có khả năng nắm bắt các đặc điểm phức tạp về kết cấu, hình thái và không gian của khối u.
Sau đó phản ánh hoạt động sinh học bên trong mà mắt thường không thể nhìn thấy.
Khi các đặc trưng hình ảnh này được tích hợp với dữ liệu TMB và PD-L1 thông qua các mô hình học máy, dấu ấn sinh học tổng hợp thu được cho thấy độ chính xác dự báo vượt trội so với bất kỳ chỉ số đơn lẻ nào.
Ví dụ: Giống như đánh giá một ứng viên không chỉ qua điểm số (tương đương PD-L1) mà còn xét thêm kinh nghiệm, kỹ năng mềm và phong cách làm việc để có bức tranh tổng thể luôn chính xác hơn một con số duy nhất.
Kết quả nghiên cứu cho thấy các dấu ấn sinh học dựa trên Radiomics có thể vượt trội hơn xét nghiệm PD-L1 đơn thuần trong nhận diện bệnh nhân thu được lợi ích thực sự và bền vững từ liệu pháp miễn dịch.
Điều này đặc biệt quan trọng trong các tình huống lâm sàng khi bệnh nhân có biểu hiện PD-L1 thấp có thể bị loại nhầm khỏi diện xem xét điều trị miễn dịch.
Nhờ nâng cao độ tin cậy trong chọn lựa bệnh nhân, AI giảm thiểu nguy cơ cả điều trị quá mức lẫn điều trị thiếu.
Do đó đảm bảo liệu pháp miễn dịch đến đúng tay những người có khả năng đáp ứng cao nhất, đồng thời bảo vệ những người khác khỏi các tác dụng phụ liên quan đến miễn dịch.
Nền tảng CHAI
Ung thư bàng quang không xâm lấn cơ (NMIBC) được điều trị bằng liệu pháp miễn dịch nội bàng quang BCG (Bacillus Calmette-Guérin) đặt ra một tình huống lâm sàng khó xử riêng biệt.
Dù BCG vẫn là phương pháp điều trị hiệu quả nhất cho NMIBC nguy cơ cao, một tỷ lệ đáng kể bệnh nhân tái phát bệnh sau liệu trình đầu tiên, buộc các bác sĩ phải cân nhắc xem có nên tiến hành thêm một đợt tấn công BCG lần hai hay không.
Các công cụ phân tầng nguy cơ hiện hành của Hiệp hội Tiết niệu Châu Âu (EAU) và Hiệp hội Tiết niệu Hoa Kỳ (AUA) cung cấp điểm nguy cơ dựa trên quần thể.
Tuy nhiên các mô hình này thiếu độ chi tiết cần thiết để dự báo diễn tiến riêng của từng bệnh nhân theo mức độ chính xác mà y học ung thư hiện đại đòi hỏi.
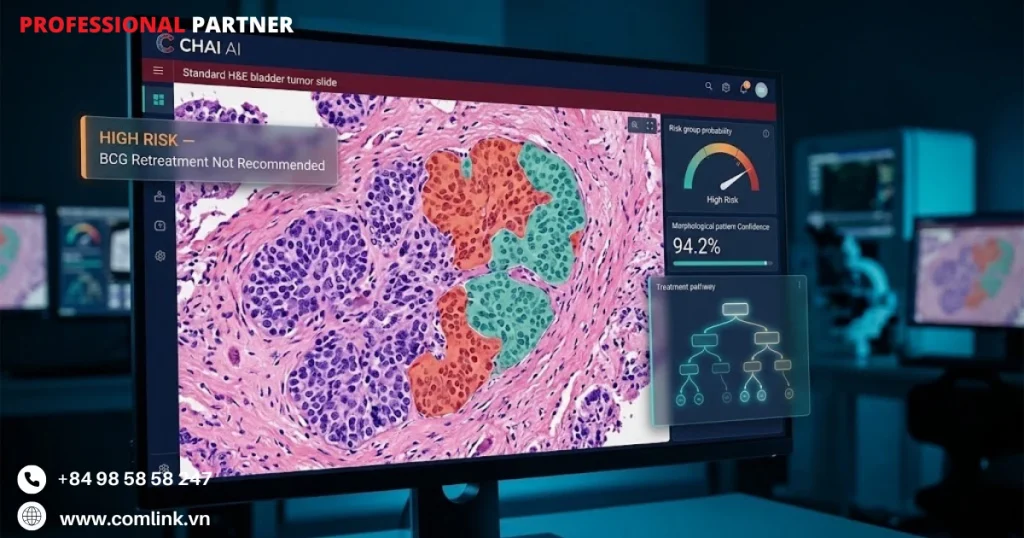
Nền tảng AI Giải phẫu Bệnh Tính toán (CHAI) lấp đầy khoảng trống này thông qua phân tích học sâu trên tiêu bản mô nhuộm Hematoxylin và Eosin (H&E) tiêu chuẩn.
Đó là loại bệnh phẩm giải phẫu bệnh phổ biến nhất trong thực hành lâm sàng.
Không cần xét nghiệm phân tử chuyên biệt hay xử lý mô bổ sung, CHAI phân tích các mẫu hình thái trong cấu trúc khối u để phân loại bệnh nhân thành các nhóm nguy cơ riêng biệt.
CHAI nhận diện những bệnh nhân ít có khả năng được hưởng lợi từ đợt tấn công BCG lần hai sau tái phát đầu tiên.
Qua đó thúc đẩy chuyển hướng kịp thời sang các liệu pháp thay thế trước khi bệnh tiến triển thêm.
CHAI hoạt động như một “bản đồ di truyền vi mô” của khối u không cần giải trình tự gene tốn kém.
Nó chỉ cần phân tích ảnh mô thông thường, nhưng vẫn đưa ra được thông tin dự báo ở cấp độ cá nhân.
Khả năng dự báo chi tiết của nền tảng này còn đi xa hơn khi những bệnh nhân mang chữ ký sinh học CHAI dương tính biểu thị tình trạng kháng BCG cho thấy kết quả điều trị tốt hơn đáng kể khi chuyển sang phác đồ kết hợp nội bàng quang.
Điều này đặc biệt có giá trị với nhóm bệnh nhân khó điều trị nhất là tổn thương Ta độ cao, nơi các mô hình EAU và AUA hiện tại cho thấy hiệu suất dự báo thấp theo lịch sử.
Khả năng chuyển hướng sớm hơn các bệnh nhân không đáp ứng BCG sang phác đồ cứu vãn hiệu quả ngay trong tiến trình bệnh của họ tương đương trực tiếp với khả năng giảm nguy cơ tiến triển và bảo tồn chức năng bàng quang.
Một số giải pháp mới trong năm 2026
| Thử nghiệm / Nghiên cứu | Thuốc / Can thiệp | Kết quả và Tác động |
|---|---|---|
| KEYNOTE-B15 | EV + Pembrolizumab | Cải thiện đáng kể OS và EFS so với Gem/Cis ở bệnh nhân MIBC. |
| IMvigor011 | Atezolizumab (MRD-guided) | Cải thiện DFS ở bệnh nhân ctDNA(+) sau phẫu thuật. |
| SWOG S-1602 | Tokyo-172 strain BCG | Không kém hơn TICE strain, mở rộng khả năng tiếp cận thuốc. |
| INDIBLADE Trial | Ipi/Nivo + Chemo/RT | 2 năm Bladder-Intact EFS đạt 78%, bảo tồn bàng quang hiệu quả. |
| LITESPARK-011 | Belzutifan + Lenvatinib | Cải thiện PFS hậu kháng PD1/L1 trong RCC (áp dụng tiềm năng cho UC). |
Có thể bạn quan tâm

Liên hệ

Địa chỉ
Tầng 3 Toà nhà VNCC
243A Đê La Thành Str
Q. Đống Đa-TP. Hà Nội

info@comlink.com.vn

Phone
+84 98 58 58 247











